
2017年1月19日,美国食品和药物管理局(FDA)已批准IMBRUVICA ®(伊布替尼)用于治疗复发难治性边缘区淋巴瘤(MZL),适用人群是那些既往使用了至少一种以抗CD20靶向药为基础方案治疗的患者。伊布替尼成为了针对“复发难治边缘区淋巴瘤”的首款FDA获批药物。
MZL是一种生长缓慢的B细胞淋巴瘤,一般出现在淋巴结和各种组织的边缘(包括胃、唾液腺、甲状腺、眼睛、肺和脾脏)的白细胞中。MZL约占所有非霍奇金淋巴瘤病例的12%。
伊布替尼此次获批用于治疗边缘区淋巴瘤,是基于一项名叫PCYC-1121的多中心、开放标签、单臂、临床II期试验数据。这个试验招募了63名复发难治性治疗边缘区淋巴瘤患者,包括所有3种亚型:黏膜相关淋巴组织(MALT; n=32),淋巴结MZL(NMZL; n=17)和脾MZL(SMZL; n=14)。试验评估了伊布替尼的安全性和有效性。结果由独立审查委员会(IRC)根据国际工作组对恶性淋巴瘤标准采用的标准进行评估,结果显示总缓解率(ORR)为46%,42.9%的患者达到部分缓解(PR)。3.2%的患者达到完全缓解。在所有三种MZL亚型中观察到总缓解率(ORR)分别为46.9%,41.2%和50.0%。这些数据在2016年12月的第58届美国血液学会(ASH)年会已报告。
来自Janssen的全球肿瘤部领头人Peter F. Lebowitz博士说:“此次FDA批准扩大了伊布替尼的适应症,包括复发/难治性边缘区淋巴瘤。它解决了患有这种严重血液恶性肿瘤患者的巨大需求。” “在我们长期致力于为患有血液恶性肿瘤的人提供有意义治疗方案的基础上,这一里程碑标志着伊布替尼治疗血液肿瘤的第5个适应症。基于药物作用机制基础上,我们将继续研究该药物治疗B细胞恶性肿瘤的潜力。”
伊布替尼已在FDA屡次获批,边缘区淋巴瘤适应症是伊布替尼获批适用的第5大血液肿瘤。到目前为止,FDA已批准其用于治疗慢性淋巴细胞白血病(CLL)、小淋巴细胞淋巴瘤(SLL)、华氏巨球蛋白血症(WM)和套细胞淋巴瘤(MCL)以及最新获批的慢性移植物抗宿主病(cGVHD)。
如需了解更多淋巴瘤的前沿信息 请扫描二维码访问“淋巴瘤亿刻”网站。

 热门推荐
MORE
热门推荐
MORE

专家“亿”周谈——直击伊布替尼,纵观CLL治疗从免疫化疗到个体化靶向疗法的革新
07-09
J HEMATOL ONCOL:前瞻性研究预测伊布替尼治疗过程中房颤的发生
07-19
CANCER CHEMOTH PHARM :PH调节剂奥美拉唑对伊布替尼影响几何?
08-08
以数据为准绳,中国新药亟需更多原始创新!——首创BTK抑制剂伊布替尼原研专家潘峥婴专访
09-30
欧洲血液学杂志:TEC与BTK抑制剂出血副作用无关
10-22
2018年IWWM 会议现场直达:伊布替尼治疗华氏巨球蛋白血症突破性进展!
11-02
专家“亿”周谈—— J CLIN ONCOL:伊布替尼单药治疗症状型/初治型华氏巨球蛋白血症的最新突破
04-09
BLOOD:基于伊布替尼的联合方案治疗复发/难治CNS淋巴瘤效果显著
05-14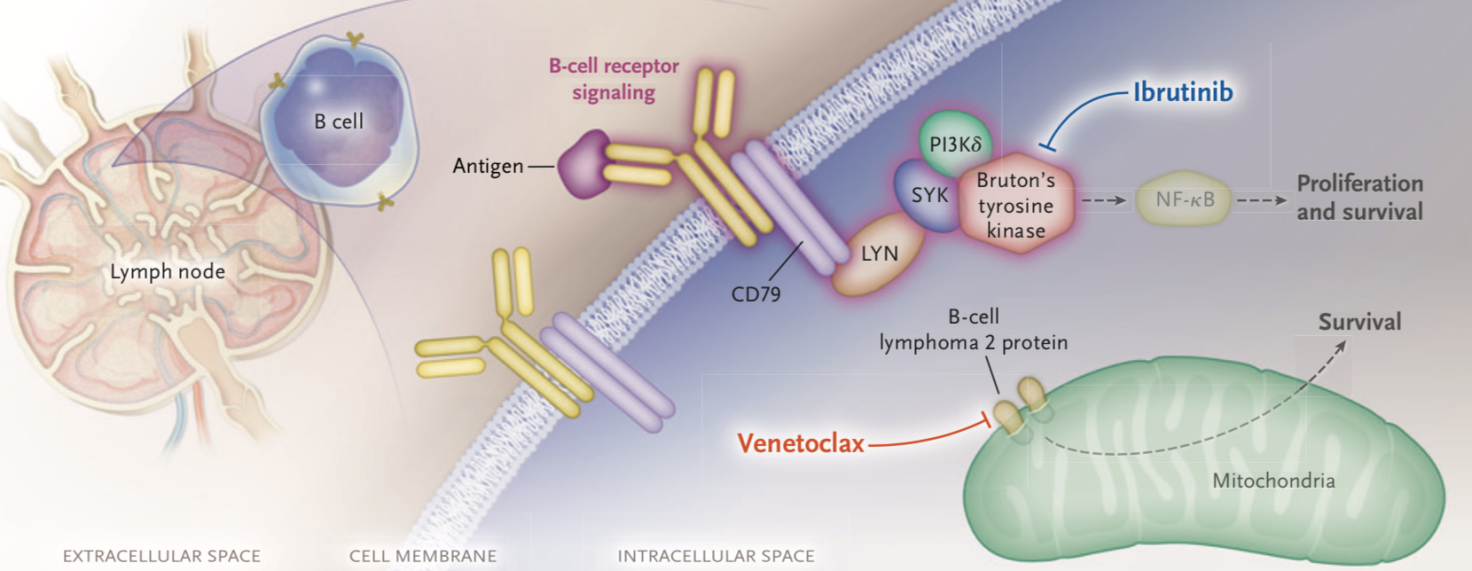
专家“亿”周谈——NEJM:伊布替尼联合维奈托克一线治疗慢性淋巴细胞白血病
06-12
【2019 ICML】黄慧强教授点评:IR联合短疗程R-HYPERCVAD / MTX在初治年轻MCL患者中有效性显著
06-20
【2019 EHA】纵览伊布替尼联合用药进一步提升CLL疗效
06-24
【2019 ICML】邱录贵教授点评:伊布替尼治疗华氏巨球蛋白血症的最新进展
06-25
【2019 ICML】张会来教授点评:伊布替尼联合利妥昔单抗治疗MCL疗效显著
06-25
【2019 ICML & EHA 回顾】中外专家畅谈伊布替尼治疗淋巴瘤的前沿进展
07-09Copyright 2008-2019 梅斯(MedSci)备案号 沪ICP备14018916号-1
