
来源:梅斯医学 2017-12-5

伊布替尼现已批准用于未经治疗的或复发型慢性淋巴细胞白血病(CLL)患者的治疗,大部分患者接受伊布替尼疗法后具有较高的治疗响应和持久响应时间。II期临床数据显示,伊布替尼联合利妥昔单抗对于慢性淋巴细胞白血病高风险患者具有极高的客观响应(ORR 95%)。近日研究人员比较了伊布替尼联合利妥昔单抗与伊布替尼单药对慢性淋巴细胞白血病患者的疗效差异。
研究招募206名慢性淋巴细胞白血病患者,随机进入伊布替尼单药组(Ib, n= 102)或伊布替尼联合利妥昔单抗组(Ib+R, n= 104),其中包含CLL复发患者以及未经治疗的高风险患者(del17p或 TP53突变, n=27)。Ib组患者接受420 mg 伊布替尼每天1次,直到出现不可接受的严重不良事件、疾病进展或死亡。Ib+R组在伊布替尼治疗基础上,治疗的前6个月接受利妥昔单抗(第1轮持续4周,每周375 mg/m2,之后每月进行2-6轮利妥昔单抗化疗)。研究的主要终点是无进展生存期,次要终点包括治疗响应,安全性以及耐受性。
患者平均年龄65岁,其中男性占70%,del17p 或TP53突变患者占70% ,del11q突变占20%,IgHV野生型患者占72%,高级阶段疾病进展患者(Rai 3-4期)占38%。基线时患者平均绝对淋巴细胞计数(ALC)为30x109/L,β2微球蛋白浓度3.7 mg/L。Ib组以及Ib+R组分别随访25.2个月和22.7个月。188名患者进行治疗响应评估。Ib组20名患者(21%),Ib+R组26名患者(28%)实现完全缓解(CR),部分缓解患者分别为72人(77%)和68人(72%)。Ib组客观响应率为98%,Ib+R组为100%。骨髓流式细胞检测显示,Ib+R组CLL微小疾病残留率更低(4.9% vs 17.1%)。Ib+R组5名微小残留阴性患者实现完全缓解,而Ib组仅1人。Ib+R组患者实现淋巴细胞绝对计数正常化(ALC, ≤4.0 K/uL)的中位时间更短(3.0 vs. 8.9 个月, p&&&&&&&&&&<0.001),实现完全缓解的平均时间缩短(11.5 vs 21.1个月; p=0.032),但组间患者无进展生存率无显著差异(91.2% vs. 90.4%, p=0.788)。56名患者终止研究,其中Ib组23人,Ib+R组33人,毒副作用是最常见的研究终止因素(n=28),研究中5名患者死亡,死亡原因分别为肾功能衰竭、脑出血、肠穿孔、结肠血肿、肺炎和呼吸衰竭。8名患者出现疾病进展,Ib组5人,Ib+R组3人,3名患者在治疗11-16个月后出现复发。6名患者出现第二恶性肿瘤,包括结直肠癌、脂肪肉瘤、多形性肉瘤样癌以及黑色素瘤,2名患者新发慢性粒细胞白血病。组间不良事件率相近,包括动脉高血压、中性粒细胞减少、腹泻和房颤。
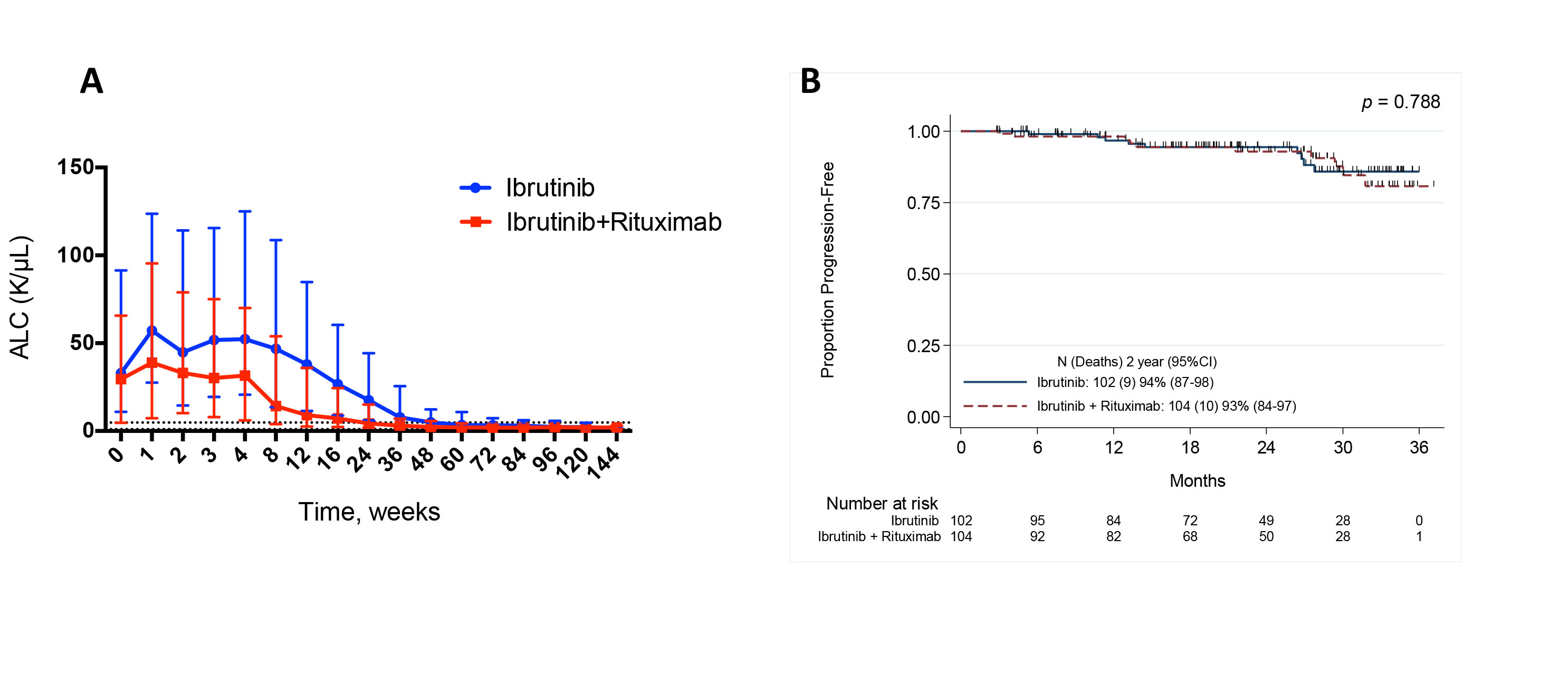
研究认为,对于复发性以及高风险慢性淋巴细胞白血病患者,接受伊布替尼联合利妥昔单抗治疗不会改善患者无进展生存期,但联合治疗会缩短患者实现治疗缓解所需时间,降低微小残留水平。
原文链接:https://ash.confex.com/ash/2017/webprogram/Paper107661.html
如需了解更多淋巴瘤的前沿信息
请扫描二维码访问“淋巴瘤亿刻”网站。

 热门推荐
MORE
热门推荐
MORE

专家“亿”周谈——直击伊布替尼,纵观CLL治疗从免疫化疗到个体化靶向疗法的革新
07-09
J HEMATOL ONCOL:前瞻性研究预测伊布替尼治疗过程中房颤的发生
07-19
CANCER CHEMOTH PHARM :PH调节剂奥美拉唑对伊布替尼影响几何?
08-08
以数据为准绳,中国新药亟需更多原始创新!——首创BTK抑制剂伊布替尼原研专家潘峥婴专访
09-30
欧洲血液学杂志:TEC与BTK抑制剂出血副作用无关
10-22
2018年IWWM 会议现场直达:伊布替尼治疗华氏巨球蛋白血症突破性进展!
11-02
专家“亿”周谈—— J CLIN ONCOL:伊布替尼单药治疗症状型/初治型华氏巨球蛋白血症的最新突破
04-09
BLOOD:基于伊布替尼的联合方案治疗复发/难治CNS淋巴瘤效果显著
05-14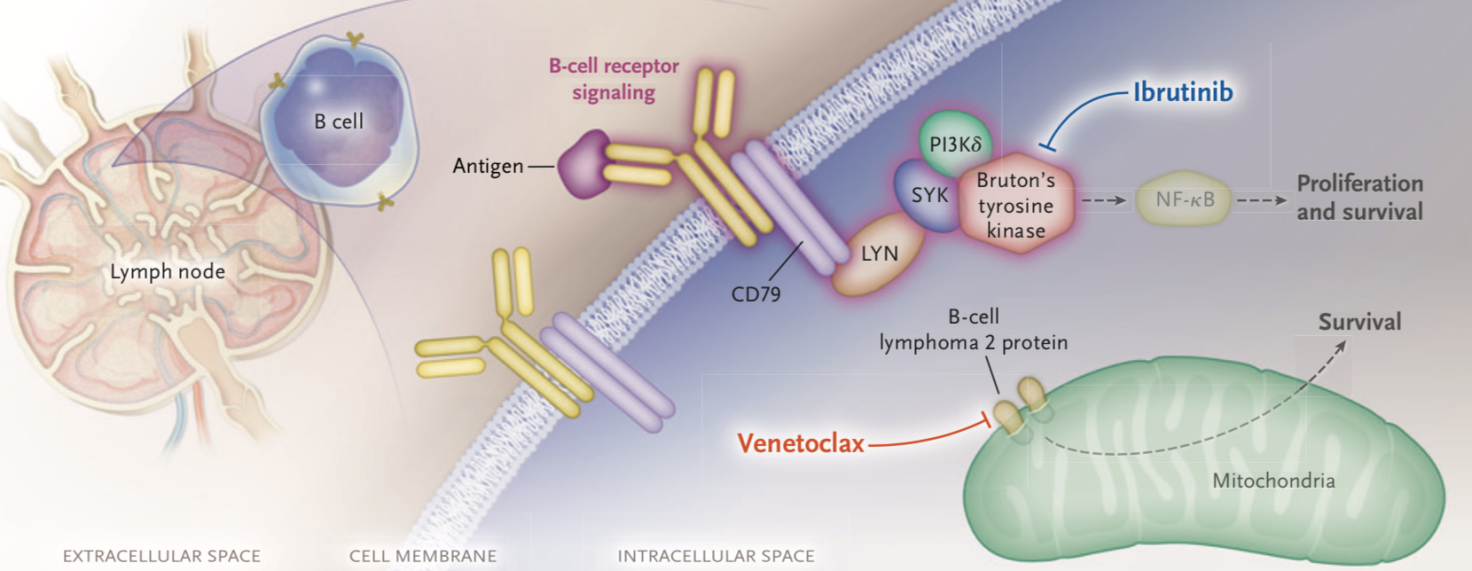
专家“亿”周谈——NEJM:伊布替尼联合维奈托克一线治疗慢性淋巴细胞白血病
06-12
【2019 ICML】黄慧强教授点评:IR联合短疗程R-HYPERCVAD / MTX在初治年轻MCL患者中有效性显著
06-20
【2019 EHA】纵览伊布替尼联合用药进一步提升CLL疗效
06-24
【2019 ICML】邱录贵教授点评:伊布替尼治疗华氏巨球蛋白血症的最新进展
06-25
【2019 ICML】张会来教授点评:伊布替尼联合利妥昔单抗治疗MCL疗效显著
06-25
【2019 ICML & EHA 回顾】中外专家畅谈伊布替尼治疗淋巴瘤的前沿进展
07-09Copyright 2008-2019 梅斯(MedSci)备案号 沪ICP备14018916号-1
